ELISA en rumiantes: fundamentos para interpretar la serología
(Publicación)
–
(Actualización)
¿Realmente le interesa al veterinario clínico un conocimiento más pormenorizado de los procedimientos serológicos que utiliza el laboratorio o le basta con recibir del mismo un resultado positivo o negativo? ¿Quién hace el diagnóstico final: el laboratorio o el clínico?
En base a nuestra experiencia desde el laboratorio, creemos que existen carencias en los conocimientos de muchos veterinarios clínicos para una correcta y completa interpretación de los resultados serológicos. Existen una serie de suposiciones que en algunos casos son erróneas y en otros como mínimo atrevidas. Por un lado, se tiende a considerar que un resultado positivo en una serología se corresponde necesariamente con un animal infectado. Es un postulado fácil de rebatir, dado que hay enfermedades que producen una seroconversión y una posterior resolución de la enfermedad, por lo que los animales seropositivos han vencido en su mayoría a la infección. Sin embargo, es también osado presuponer que un animal positivo es en el cien por cien de los casos un animal que ha tenido contacto con un microorganismo, dado que las propias técnicas serológicas tienen limitaciones técnicas y por tanto márgenes de error.
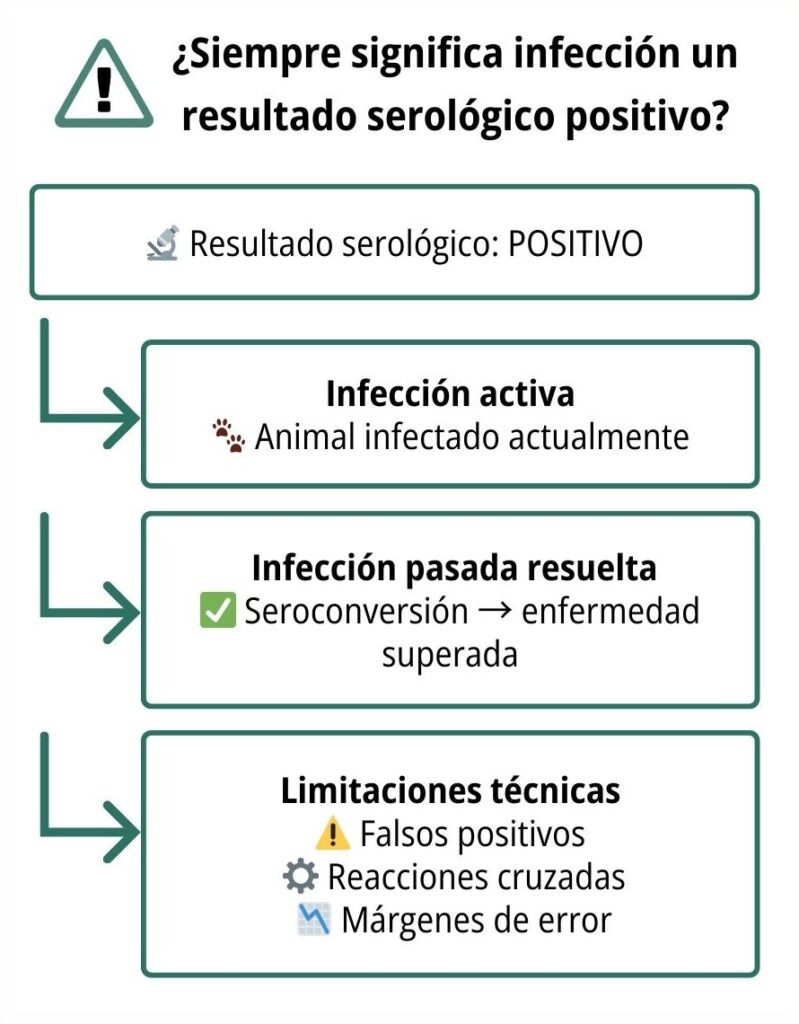
Figura 1. Posibles interpretaciones de un resultado serológico positivo.
Un mejor conocimiento de la técnica serológica, unido al conocimiento de la enfermedad que tienen los veterinarios clínicos, puede conducir a una mejor interpretación de los resultados serológicos y de su utilidad en el diagnóstico y control de las enfermedades.
La técnica ELISA
La técnica ELISA es una reacción antígeno-anticuerpo asociada a una reacción enzimática, que tiene como final una lectura colorimétrica. En el ELISA indirecto, que es una de las metodologías ELISA más comunes, se utilizan pocillos tapizados con un antígeno, a los que se añade la muestra de suero. Si hay anticuerpos específicos en ella, se unen al antígeno y se fijan al pocillo. Posteriormente se añade un conjugado consistente en un antianticuerpo que va unido a una enzima, y que reacciona con los anticuerpos de la muestra. Finalmente se añade un sustrato que si es metabolizado por mediación de la enzima, se produce una reacción de color, que es medida a través de un espectrofotómetro a determinada longitud de onda. Si hay suficiente color, la muestra es positiva.
Otros métodos de ELISA utilizados con frecuencia son los de bloqueo o de competición. En ellos, además de la muestra se añade otro anticuerpo que va a competir con ella para fijarse al antígeno. Si la muestra de suero tiene anticuerpos, éstos se unirán al antígeno, impidiendo que lo haga el anticuerpo complementario. Dado que el conjugado y la reacción del enzima-sustrato están ligados al anticuerpos complementario o “competidor”, la presencia final de color significará, a diferencia de los métodos indirectos, que la muestra es negativa.
En todos los ELISAS, además de las muestras se inocularan controles positivos y negativos, que servirán de referencia para el cálculo de resultados del test.
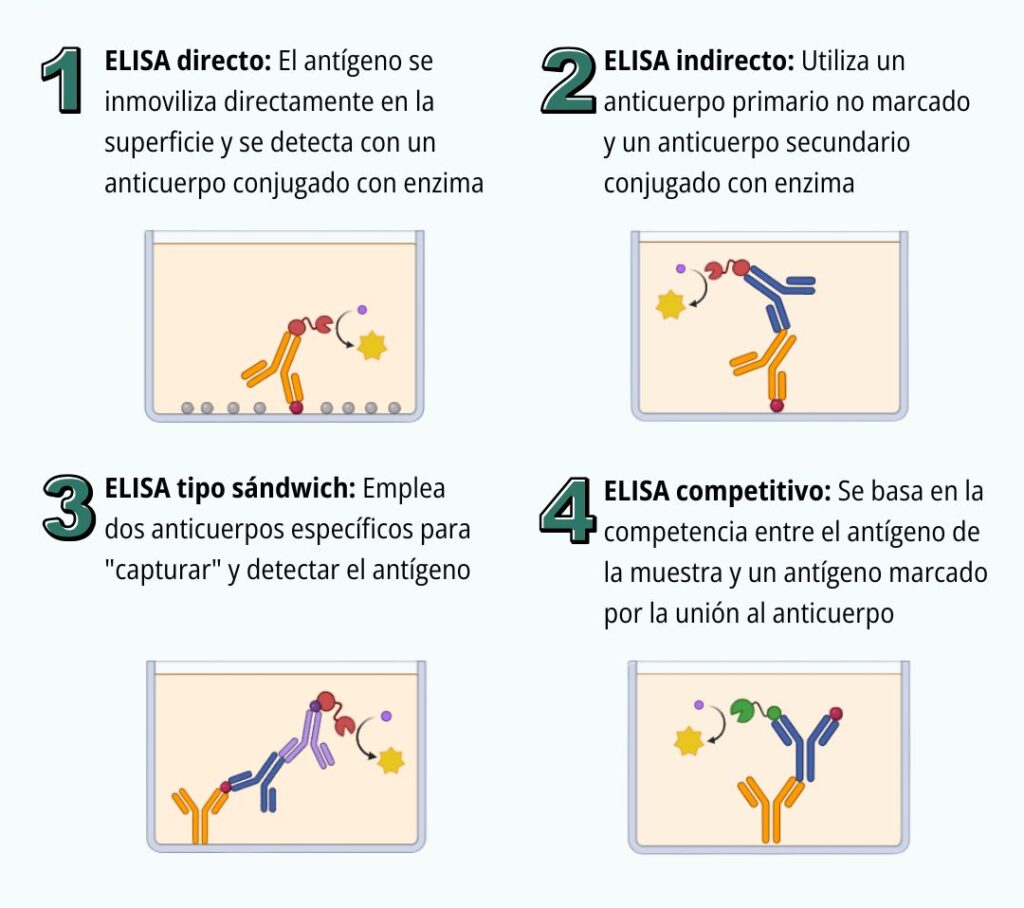
Figura 2. Principales tipos de ELISA.
Tras la lectura colorimétrica, el equipo arroja para cada muestra da un valor numérico denominado “densidad óptica”. El cálculo del resultado de una muestra concreta se realiza en base a los resultados del control positivo, del control negativo o, normalmente, de ambos. En los ELISA indirectos, normalmente se calcula el cociente entre la densidad óptica de la muestra y a la densidad óptica del control positivo, de forma que la positividad de la muestra es directamente proporcional al valor numérico que aparece en el informe de resultados. Por el contrario, en los ELISA de competición suelen ser al revés. El valor final del ELISA o “porcentaje de inhibición” se calcula en base al cociente entre la densidad óptica de la muestra y la densidad óptica del control negativo, por lo que el resultado final o índice de ELISA es inversamente proporcional a la cantidad de anticuerpos que tiene ese animal en sangre.

Figura 3. Métodos de cálculo más habituales en función del tipo de ELISA
Tras la lectura colorimétrica, el equipo arroja para cada muestra da un valor numérico denominado “densidad óptica”. El cálculo del resultado de una muestra concreta se realiza en base a los resultados del control positivo, del control negativo o, normalmente, de ambos. En los ELISA indirectos, normalmente se calcula el cociente entre la densidad óptica de la muestra y a la densidad óptica del control positivo, de forma que la positividad de la muestra es directamente proporcional al valor numérico que aparece en el informe de resultados. Por el contrario, en los ELISA de competición suelen ser al revés. El valor final del ELISA o “porcentaje de inhibición” se calcula en base al cociente entre la densidad óptica de la muestra y la densidad óptica del control negativo, por lo que el resultado final o índice de ELISA es inversamente proporcional a la cantidad de anticuerpos que tiene ese animal en sangre.
Existe la tendencia de referirse al resultado de un ELISA como “título de anticuerpos”, cuando en realidad dicho resultado no se expresa en forma de “título”. La titulación de un suero requiere hacer diluciones seriadas, de forma que el título de la muestra se corresponde con la última dilución que resulta positiva en la prueba serológica. Por el contrario, en las pruebas de ELISA rutinarias, el resultado numérico arrojado no es estrictamente “cuantitativo”, ni comparable entre diferentes ELISA de una misma enfermedad.
Interpretación a nivel de individuo
a) Limitaciones de la técnica. Sensibilidad y especificidad.
Después de obtener un resultado numérico en el ELISA, resta calificar a los animales como enfermos o sanos, lo cual se realiza en función de un “punto de corte”, valor por encima del cual se considera positiva a la muestra y por debajo del cual se considera negativa. Este punto de corte viene establecido normalmente por la empresa fabricante del kit, en base a estudios de correlación con otras pruebas de referencia. El problema es que en la distribución de las densidades ópticas de los resultados de ELISA en animales sanos y animales enfermos hay un cierto solapamiento, es decir, hay animales enfermos que tienen un valor de ELISA inferior que algunos animales sanos o, lo que es lo mismo, animales sanos con valores de ELISA superiores a algunos animales enfermos. Así, el punto de corte se suele fijar en valores que permitan el máximo número posible de animales correctamente calificados, buscando el óptimo “equilibrio” entre especificad y sensibilidad.
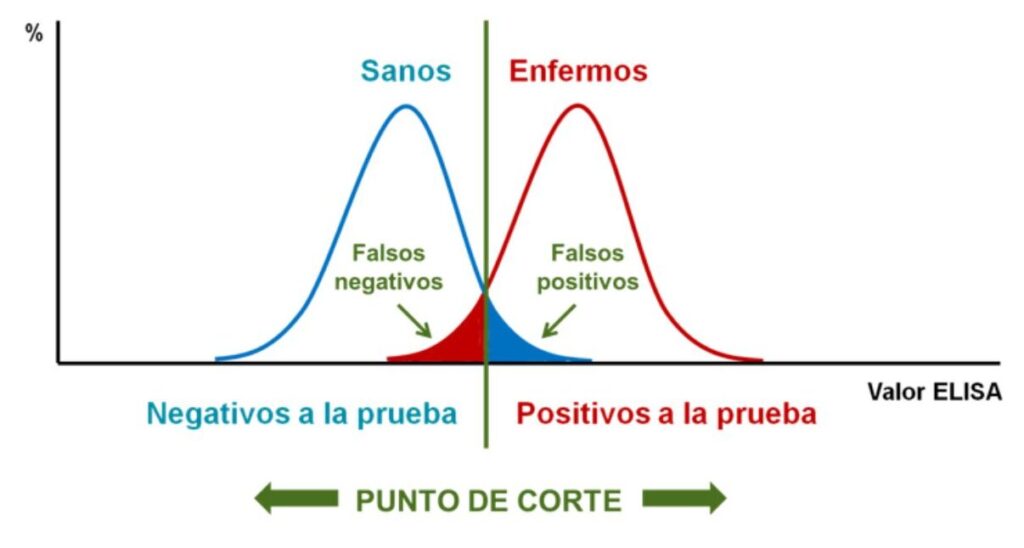
Figura 4. Distribución de valores de ELISA en animales sanos y enfermos y
establecimiento del punto de corte, con solapamiento entre ambas poblaciones.
A efectos de explicación de los parámetros de eficacia de la técnica, nos referiremos a “animal enfermo” como aquel que verdaderamente ha tenido un contacto con el patógeno (con independencia de que en ese momento esté o no infectado) y que por tanto tiene anticuerpos específicos en sangre, mientras que nos referiremos a “animal sano” como aquel que no ha estado expuesto al patógeno y que por tanto no presenta anticuerpos específicos en sangre.
Si el laboratorio informa únicamente del resultado positivo o negativo pero no facilita el valor numérico del ELISA ni el punto de corte del test, el clínico desconocerá qué animales están muy cerca del punto de corte, por encima o por debajo, individuos que corren un mayor riesgo de quedar mal calificados: individuos enfermos que son negativos y sanos que son positivos, denominados “falsos negativos” y “falsos positivos” respectivamente.
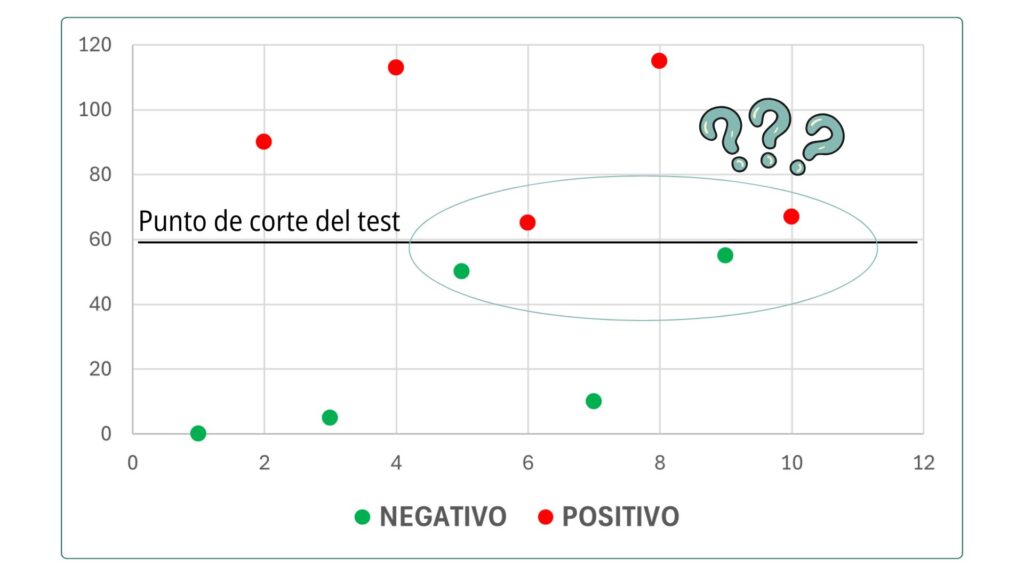
Figura 5. Muestras con valores próximos al punto de corte del ELISA,
donde aumenta la probabilidad de falsos positivos y falsos negativos.
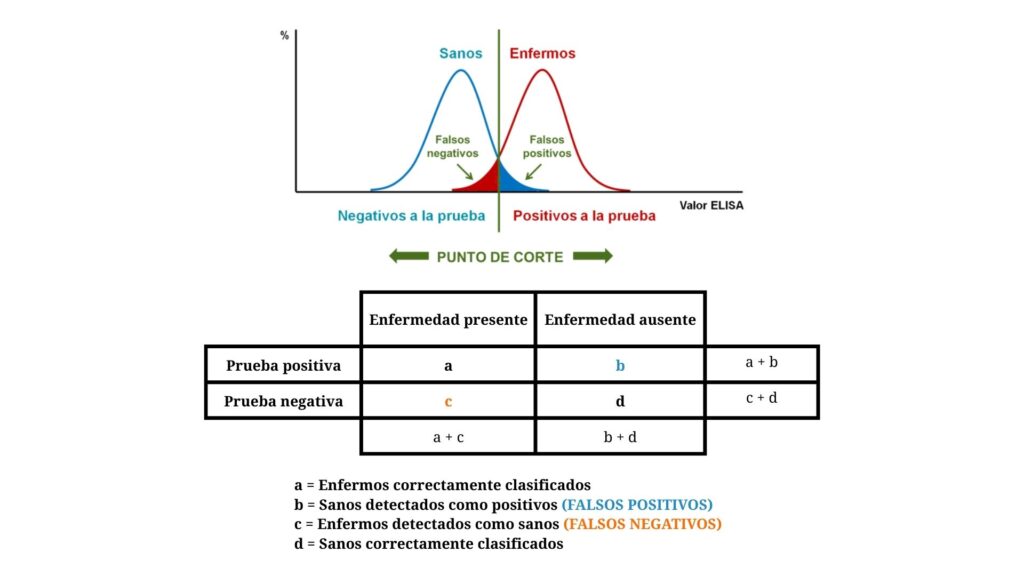
Figura 6. Definición y cálculo de los falsos positivos y negativos.
Partiendo de esta base, se deben conocer los dos parámetros básicos que deben acompañar a cada técnica diagnóstica: la sensibilidad y la especificidad. La sensibilidad de un kit es la probabilidad de que un animal enfermo sea detectado. La especificidad es la probabilidad de que un animal sano sea negativo al test. Sin embargo, la sensibilidad y la especificidad de los kits comerciales es en muchos casos desconocida ya que no viene referenciada en las instrucciones técnicas del kit. Se puede pedir información a las casas comerciales, la cuales proporcionan informes técnicos al respecto, pero realmente no hay un organismo normalizador que ofrezca a los laboratorios suficientes garantías en parámetros como sensibilidad, especificidad o concordancia entre los diferentes kits. Los rangos de especificidad habituales pueden situarse entre el 95% y el 100%. Sin embargo, hay que ser conscientes de que un valor de 99,5% parece una buena especificidad, pero significa que de cada 200 animales sanos, uno va a dar positivo en el ELISA.
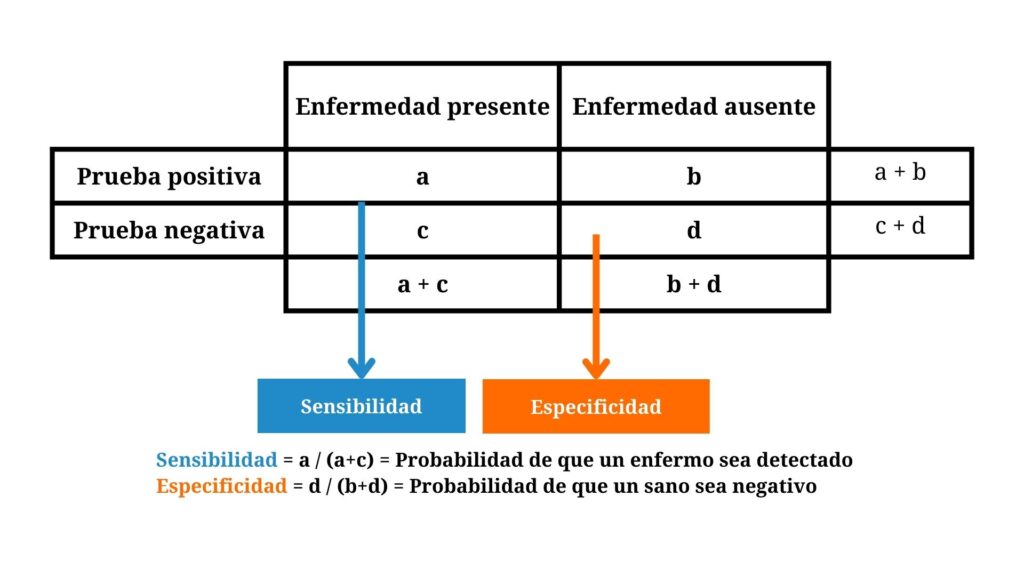
Figura 7. Definición y cálculo de la sensibilidad y especificidad.
b) Causas de falsos positivos y falsos negativos ajenas a la técnica
Al margen de las limitaciones ligadas a la propia técnica (calidad de los antígenos utilizados, robustez del diseño, etc.), que se escapan del control del veterinario clínico, existen diversas causas ligadas tanto al animal como al patógeno que provocan errores en la correcta calificación de los animales como sanos o enfermos.
En el caso de los falsos negativos, pueden existir animales enfermos seronegativos en las siguientes circunstancias:
– Animales inmunodeprimidos en fases terminales de enfermedad
– Animales que nacen infectados sin capacidad de generación de anticuerpos (inmunotolerancia congénita)
– Animales en fase muy precoz de la enfermedad, en la que aún no hay producción de IgG detectables, fases de negatividad serológica que pueden alargarse durante meses o años en enfermedades como la Paratuberculosis.
– Animales infectados crónicamente en los que hay periodos de baja exposición inmune al patógeno y descenso de los anticuerpos circulantes en sangre.
En el caso de los falsos positivos, existen animales sanos seropositivos en las siguientes circunstancias:
– Animales con presencia en sangre de anticuerpos vacunales, normalmente indistinguibles de los anticuerpos generados por la infección natural.
– Animales con presencia en sangre de anticuerpos calostrales. Es necesario mantener un periodo de espera desde el nacimiento hasta los 4-6 meses a fin de garantizar que los anticuerpos detectados no tengan un origen materno.
– En función de la patogenia de los distintos microorganismos, hay agentes que infectan a un animal para toda la vida, y por lo tanto la positividad siempre está ligada a la infección, (Paratuberculosis, CAEV), otros que producen infecciones agudas pasajeras y por tanto generan anticuerpos que pueden perdurar indefinidamente sin estar ligados a la existencia de infección (Toxoplasma, Virus Border) y otros en los que es difícil saber si ha existido resolución de la infección o cronicidad sin recurrir a otras técnicas diagnósticas (Agalaxia Contagiosa, Fiebre Q).
c) Valor predictivo
Otro parámetro que debe conocer el veterinario de campo es el “valor predictivo”. El margen de error del ELISA se puede de expresar de forma más práctica para el clínico como:
– “Valor predictivo del positivo”: probabilidad de que un animal positivo al ELISA sea realmente un animal enfermo (distinto de la sensibilidad, que era la probabilidad de que un animal enfermo dé positivo en el test).
– “Valor predictivo del negativo”: probabilidad de que un animal negativo al ELISA sea realmente un animal sano (distinto de la especificidad, que era la probabilidad de que un animal sano diera negativo en el test).
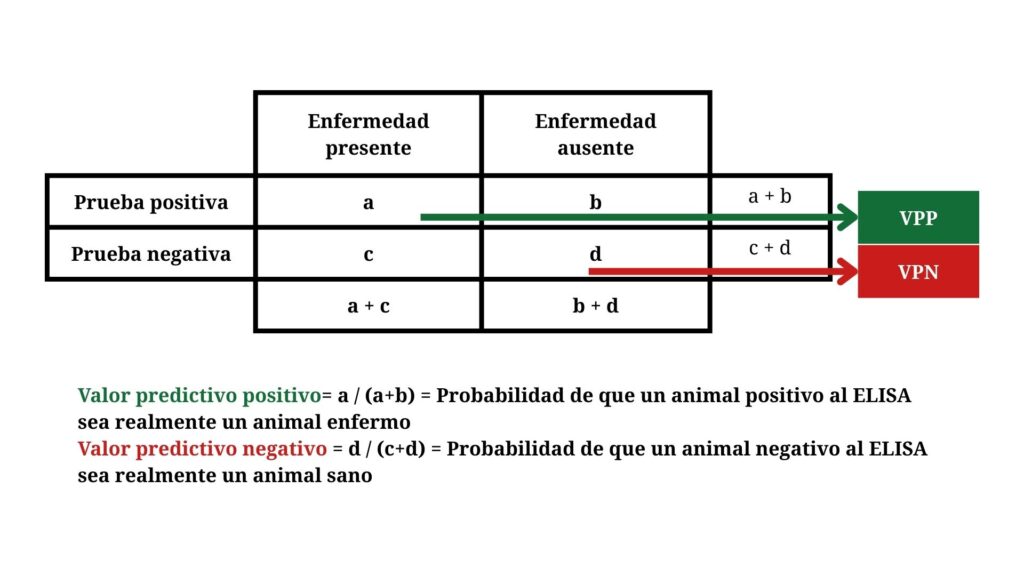
Figura 8. Definición y cálculo de los valores predictivos positivo y negativo.
Una particularidad del valor predictivo, a diferencia de la sensibilidad y la especificidad, es que no depende exclusivamente de la técnica. El valor predictivo varía también en función de la prevalencia y es algo que debe tenerse en cuenta a la hora de interpretar resultados. El valor predictivo positivo va aumentando a medida que aumenta la prevalencia de una enfermedad en el rebaño. Así, cuanta más prevalencia hay en el rebaño, más probabilidad hay de que el positivo del laboratorio sea un animal enfermo. Con el valor predictivo negativo ocurre lo contrario: a medida que aumenta la prevalencia en el rebaño, la probabilidad de que ese resultado negativo sea realmente un animal sano, va disminuyendo hasta valores que no son despreciables. Si se tiene una prevalencia del 50%, el valor predictivo negativo baja del 100% al 90% aproximadamente, es decir, de cada 10 animales negativos, uno esté probablemente infectado. Este hecho explica que, cuando se empiezan a hacer chequeos serológicos en una explotación con prevalencias muy alta, con el objetivo de detectar animales positivos, a medida que se hacen muestreos secuenciales, se siguen encontrando animales positivos, porque el valor predictivo negativo en las fases iniciales de alta prevalencia es menor. Cuando se tienen prevalencias más bajas, se tiene un alto valor predictivo negativo y menor valor predictivo positivo.
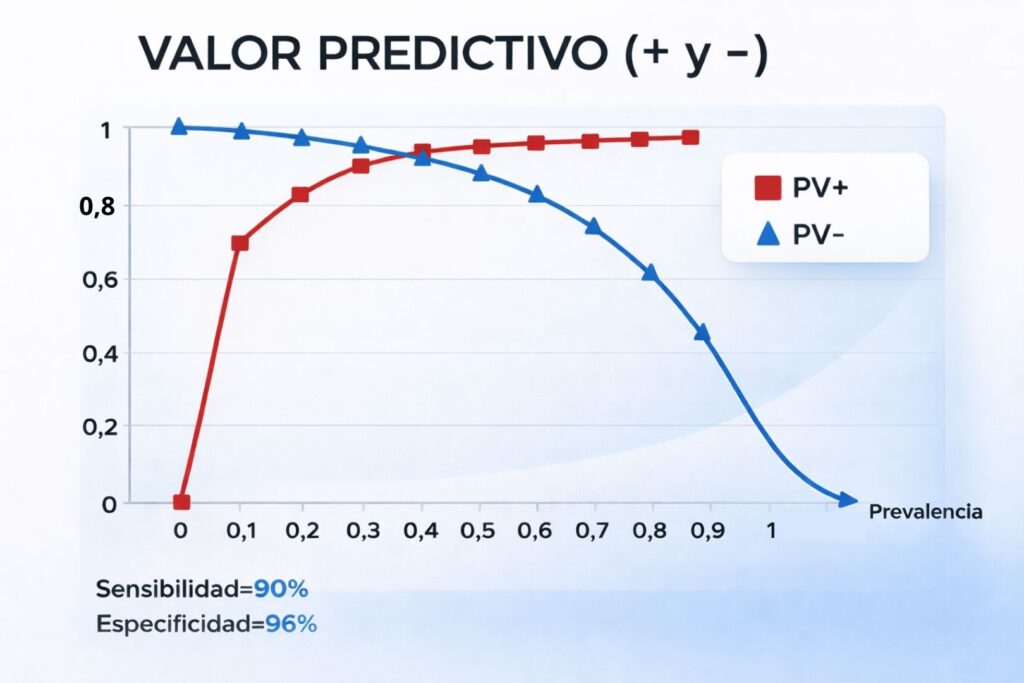
Figura 9. Evolución del valor predictivo positivo y negativo según
la prevalencia del rebaño.
En los resultados de un informe, el punto de corte viene establecido por el laboratorio, pero el veterinario clínico, en base a todo lo explicado, puede desplazarlo a voluntad, bajándolo para aumentar la sensibilidad (en detrimento de la especificidad) o subiéndolo para aumentar la especificidad (en detrimento de la sensibilidad), en función de los intereses concretos establecidos para el control sanitario de un determinado proceso. Así, puede interesar bajar algo el punto de corte en estudios de ‘screening’ o en programas de erradicación en los que dejar animales positivos supone una pérdida grave de eficacia en ese plan, por ejemplo ante una elevada contagiosidad. Por el contrario, puede interesar subir el punto de corte, aumentando la especificidad, en estudios de verificación donde interesa si saber un animal está realmente infectado, en planes de control a largo plazo y planes no estrictos o de enfermedades de baja contagiosidad que suponen el sacrificio de positivos, especialmente si los animales tienen un alto valor económico.
Interpretación a nivel de rebaño
Los estudios serológicos a nivel de rebaño tienen numerosas utilidades desde el punto de vista diagnóstico. Así, se utilizan para detectar la enfermedad (presencia de al menos un animal enfermo), calcular la prevalencia (el porcentaje de animales enfermos), calcular la incidencia (tasa de nuevas infecciones en un periodo de tiempo determinado, a través de chequeos seriados en animales previamente negativos) o valorar la posibilidad de que un patógeno concreto esté implicado en un proceso clínico (estableciendo correlaciones estadísticas entre seropositividad y presencia de enfermedad).
Obviamente, también se utiliza la serología como herramienta fundamental en programas de control y/o erradicación de enfermedades basados en el sacrificio o segregación de animales positivos.
Por último, se pueden establecer protocolos preventivos basados en serología, como el análisis de animales de nueva incorporación al rebaño o el mantenimiento de ‘poblaciones centinela’ que permita una detección precoz de la entrada de un patógeno.
Cuando se intenta calificar un rebaño como sano o enfermo en base a un muestreo serológico, se aumenta la sensibilidad y se disminuye la especificidad a medida que se incluyen más animales en el muestreo. Por ejemplo, si se tiene una sensibilidad del 95% y una especificidad del 99% y se analiza una muestra en un rebaño de 100 individuos que tiene una prevalencia 0, la probabilidad de que un animal negativo esté sano es del 99%, coincidiendo con la especificidad de la técnica.
Este efecto es acumulativo y, a medida que se incrementa el tamaño de la muestra, baja la especificidad a nivel de rebaño. Si se analizan 10 animales, ya únicamente se tiene un 90% de probabilidades de que todas las muestras den negativo en un rebaño sano. Si se analizan los 100 animales, se tendrá tan sólo un 37% de probabilidades de que todos los animales salgan negativos.
Para limitar el problema de especificidad a nivel de rebaño, puede ser recomendable subir el punto de corte del test o el umbral de positividad del rebaño de un animal positivo a dos animales positivos como condición para calificar el rebaño como infectado. Por su parte, para limitar el problema de sensibilidad, se puede aumentar el tamaño de muestreo. Cuantos más animales se elijan, más se aumenta la probabilidad de detección de esa enfermedad en el rebaño.
Algunos ejemplos
Como aplicación práctica de todo lo expuesto anteriormente, se exponen a continuación algunos ejemplos de la forma en la que se pueden interpretar valores numéricos de ELISA conociendo las circunstancias en las que están ocurriendo:
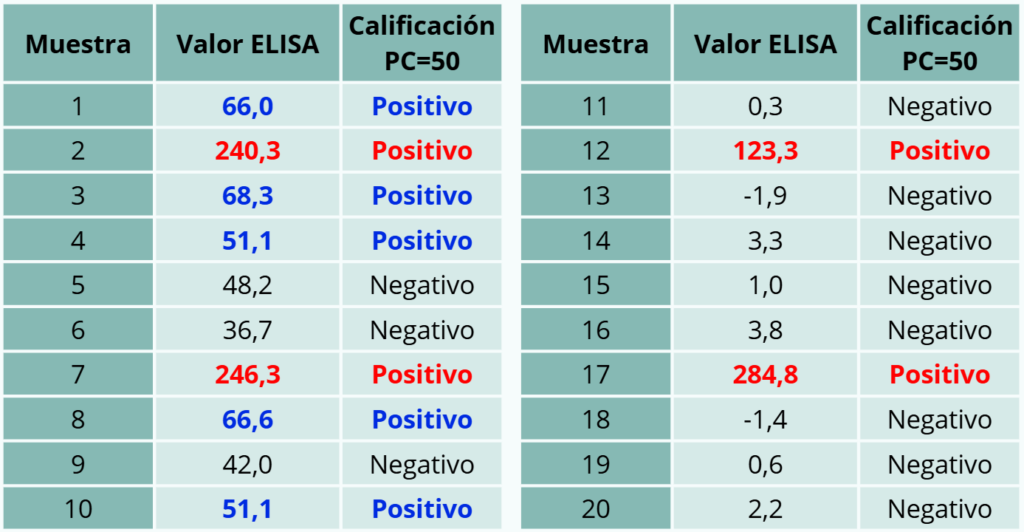
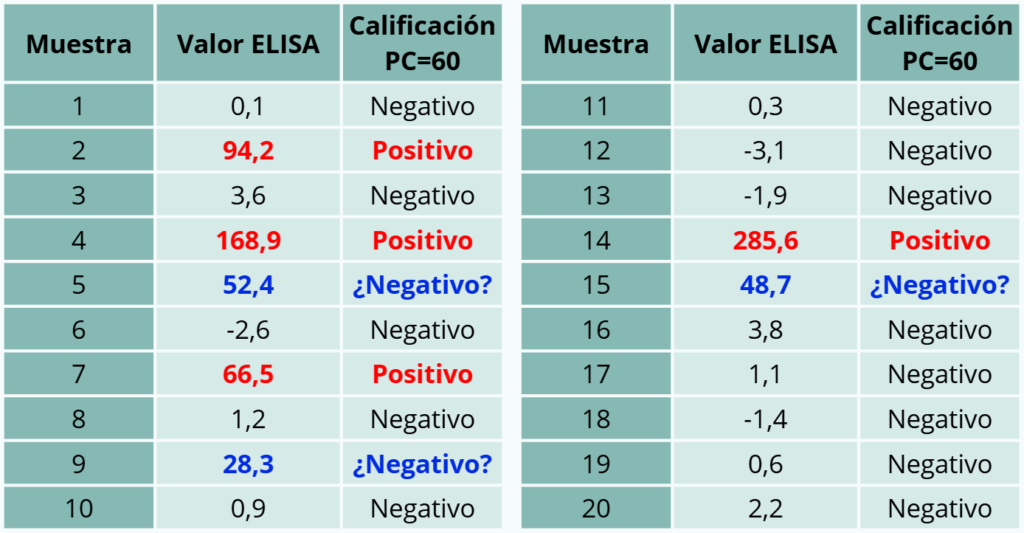
– Ejemplo 1. Serología con un punto de corte de 60. Se detectan animales con valores positivos muy altos y otros con valores negativos muy bajos. Sin embargo, el animal nº 15 es negativo con un índice de ELISA de 52,4, rozando el punto de corte y alejado del valor promedio del resto de animales negativos. En buena lógica, es un animal altamente sospechoso de estar infectado. En menor medida, también sería recomendable repetir el análisis transcurridas varias semanas en los animales nº 9 y 15.
Tabla 1. Ejemplo 1.
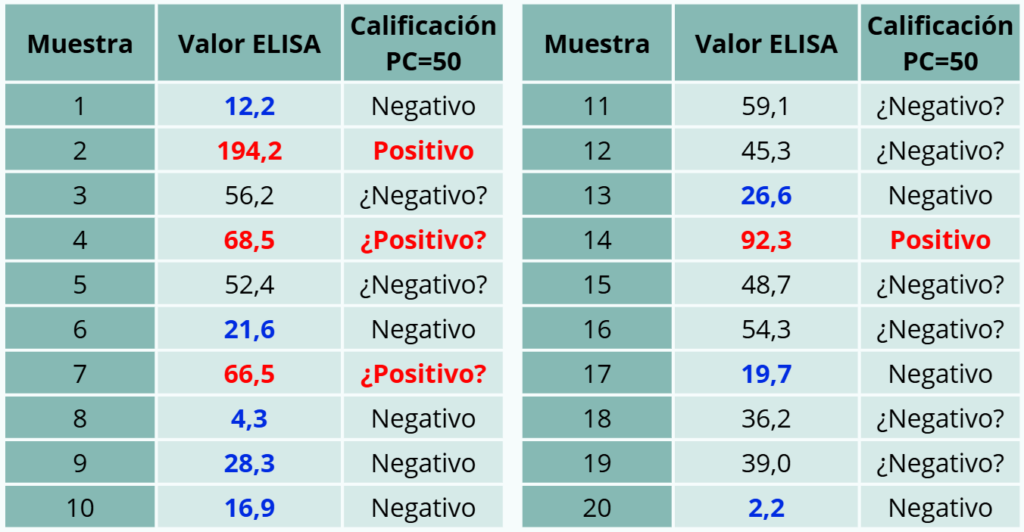
– Ejemplo 2. Serología con un punto de corte de 60. Se obtienen numerosos animales positivos muy cercanos al punto de corte y numerosos animales negativos muy cercanos al punto de corte. Son unos resultados poco robustos. No es un ELISA que esté funcionando bien en lo que se refiere a la discriminación entre animales positivos y negativos, debido a que todos están cerca del punto de corte. Se deben buscar kits de ELISA que tengan una distribución de los valores positivos y negativos mucho más diferenciada entre ambos grupos. Es normal que a medida que aumenta la prevalencia aumente el “ruido de fondo” (negativos pero cercanos al punto del corte), pero no obstante los negativos deberían ser más claros.
Tabla 2. Ejemplo 2.
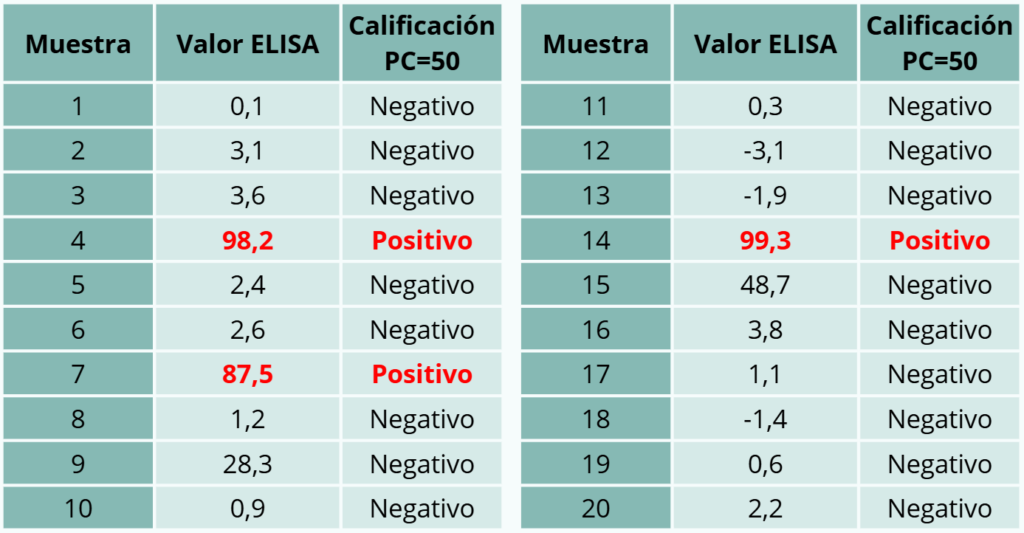
– Ejemplo 3. Búsqueda de animales seropositivos de entre 6 y 12 meses de edad con el fin de confirmar la circulación reciente de un virus en el rebaño. Si hay animales seropositivos, se puede tener la convicción de que el virus ha estado en el rebaño al menos en los últimos doce meses. Se detectan tres animales positivos, lo que permite una conclusión altamente fiable de que el virus ha circulado en el rebaño.
Tabla 3. Ejemplo 3.
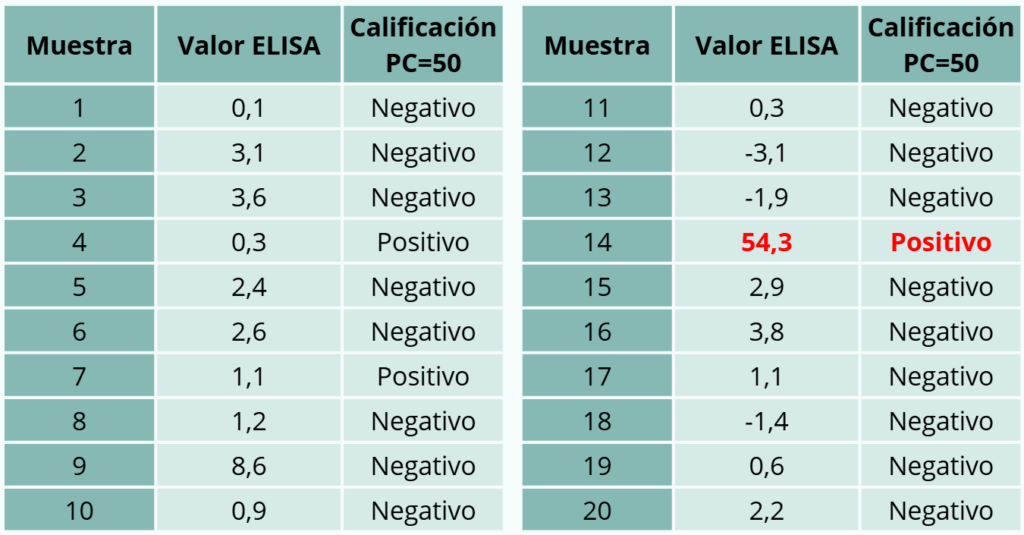
– Ejemplo 4. Búsqueda de animales seropositivos de entre 6 y 12 meses de edad con el fin de confirmar la circulación reciente de un virus en el rebaño. Si hay animales seropositivos, se puede tener la convicción de que el virus ha estado en el rebaño al menos en los últimos doce meses. El punto de corte del test es 50. Todos los animales son negativos salvo uno, que presenta un valor de 54,3. Sería arriesgado afirmar que el virus ha circulado en el rebaño dado que hay una baja seroprevalencia en el lote muestreado, el valor predictivo del positivo baja y el valor de ELISA del positivo está rozando el punto de corte. Convendría en consecuencia realizar investigaciones complementarias en la explotación.
Tabla 4. Ejemplo 4.
– Ejemplo 5. Serología en animales vacunados hace 3 meses y en animales “testigo” no vacunados. Los primeros muestran valores positivos muy altos y los segundos son todos negativos. Se concluye que la positividad es de origen vacunal y que sugiere una correcta inmunización, así como la probable no circulación del patógeno en el lote chequeado. Es muy interesante mantener poblaciones centinela sin vacunar para poder realizar chequeos periódicos y valorar si hay o no circulación de un patógeno en el rebaño.
Tabla 5. Ejemplo 5.
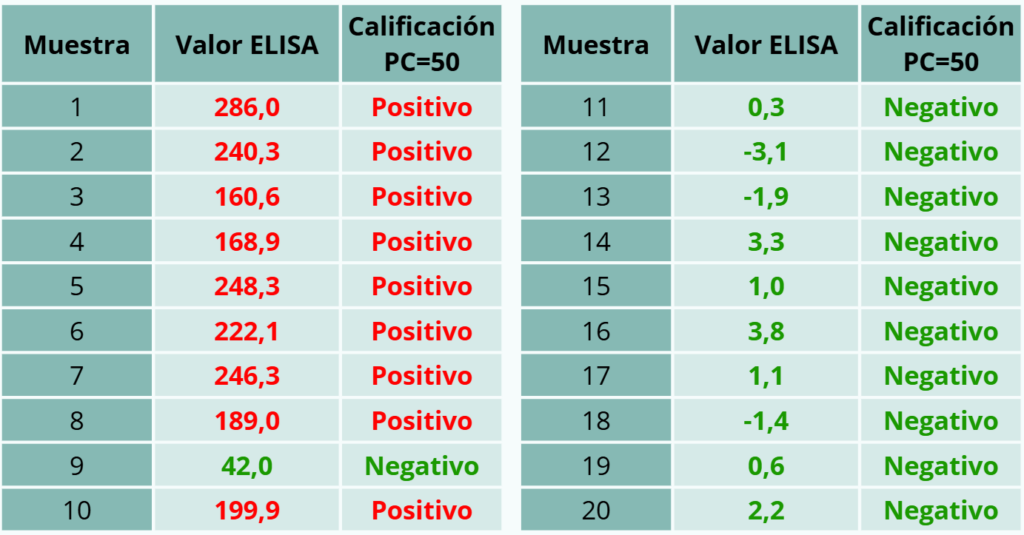
– Ejemplo 6. Serología en animales vacunados hace dos años y en animales “testigo” no vacunados. Detectamos dos animales positivos en el grupo centinela, con valores altos, lo que es un indicio firme de que ha habido circulación del patógeno. En el grupo de vacunados, hay una mayoría de animales positivos con índices relativamente bajos y varios con valores muy altos. Se puede manejar la hipótesis de que éstos últimos han tenido probablemente una infección natural, y en el resto la positividad tiene un origen vacunal residual.
Tabla 6. Ejemplo 6.